Composti organici di zolfo polivalente: solfossidi e solfoni
Due gruppi principali di composti organosolfurici che non hanno controparti tra i composti organici dell'ossigeno sono i solfossidi e i solfoni. Se il legame in questi composti è rappresentato con strutture doppiamente legate - ad esempio, ―S (= O) - per solfossido e ―S (= O) 2 - per solfone - gli atomi di zolfo “vedono” 10 e 12 elettroni di valenza, rispettivamente. Questo è più di quanto consente la regola dell'ottetto, ma lo zolfo non è vincolato dalla regola dell'ottetto, perché può utilizzare gli orbitali 3d nel suo legame, come sarebbe richiesto anche in composti come l'esafluoruro di zolfo (SF 6). Mentre esiste un supporto teorico per l'espansione del guscio di valenza di zolfo per ospitare più di otto elettroni, l'uso degli orbitali 3d negli schemi di legame è stato criticato perché gli orbitali 3d hanno un'energia molto più elevata rispetto agli orbitali di zolfo 3 e 3p. Un modello di legame alternativo invoca il legame polare come ―S + (―O -) - per solfossido e ―S 2+ (―O -) 2− per solfone. Mentre è chiaro che le strutture di risonanza polare contribuiscono al legame complessivo, è probabile che vi sia un contributo anche dagli orbitali 3d di zolfo. Va notato che il gruppo solfossido contiene anche una sola coppia di elettroni sull'atomo di zolfo, che richiede che il gruppo solfossido sia non piano, simile a un'ammina, ma abbastanza diverso dalla struttura planare di un gruppo carbonile, ―C (= O) -, a cui viene talvolta confrontato un gruppo solfossido. Una conseguenza importante della non planarità del gruppo solfossido è che i solfossidi del tipo R (S = O) R ′, dove R e R ′ sono diversi, sono chirali e possono infatti essere isolati in forma otticamente attiva, con il gruppo solfone essere tetraedrico. Contrariamente alle ammine ma simile alle fosfine, lo zolfo tricoordinato (composti trigonali di zolfo piramidale con tre ligandi e una coppia solitaria di elettroni sullo zolfo - come si trova, ad esempio, in solfinil cloruri, esteri di solfito, solfossidi, tiosolfinati e solfimi) configurazione stabile, a causa di legami più lunghi con lo zolfo (meno affollamento) e una maggiore quantità di caratteri solitari a coppia solitaria (la percentuale di orbitale s nel numero totale di orbitali utilizzati nell'ibridazione). Molti composti tricoordinati otticamente attivi si verificano in natura e i composti di zolfo otticamente attivi sono ampiamente utilizzati nella sintesi di altri composti chirali.
I solfossidi sono nominati semplicemente designando, in ordine alfabetico, i due gruppi organici collegati al gruppo ―S (= O), seguito dalla parola sulfoxide (ad esempio, etilmetil solfossido, CH 3 S (O) C 2 H 5) o formando un prefisso dal nome del più semplice dei gruppi usando la particella -solfinil- (ad esempio, acido 4- (metilsolfinil) benzoico). La nomenclatura dei solfoni è simile a quella dei solfossidi; la particella-solfonile- viene usata in casi complicati. La maggior parte dei solfossidi sono liquidi o solidi incolori con bassi punti di fusione. Il solfossido di dimetilsolfossido a basso peso molecolare (CH 3 S (= O) CH 3, DMSO) è solubile in acqua, presenta bassa tossicità ed è un solvente eccellente. Possiede la capacità insolita di penetrare rapidamente nella pelle e può trasportare composti attraverso la pelle in questo modo. Ha qualche utilità nella medicina veterinaria, in particolare nel trattamento della zoppia nei cavalli. I solfoni sono generalmente solidi cristallini incolori. Il dimetilsolfone è solubile in acqua. I diaril solfoni (pH 2 NC 6 H 4 SO 2 C 6 H 4 NH 2- p; ad es. Dapsone) e composti correlati sono stati usati nel trattamento della tubercolosi e della lebbra. Le resine di polisulfone, che incorporano l'unità ―SO 2 C 6 H 4 - all'interno di un polimero, sono utilizzate su larga scala per parti elettriche e automobilistiche e altre applicazioni che richiedono un'eccellente stabilità termica e resistenza all'ossidazione.
Evento e preparazione
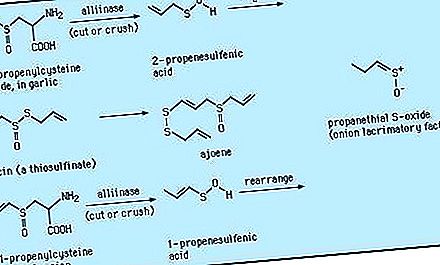
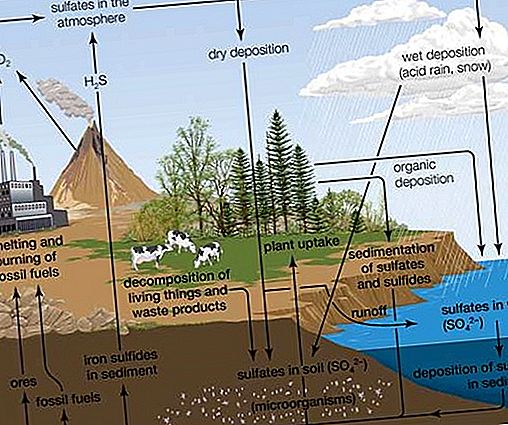
Tra i composti isolati da fonti naturali, gli S-ossidi S-alchil cisteina (come S-1- e S-2-propenilcisteina S-ossidi), i precursori degli aromatizzanti delle piante del genere Allium, furono i primi trovati ad avere attività ottica sul carbonio e su un altro elemento (zolfo). Da allora una varietà di altri solfossidi è stata isolata da fonti naturali, tra cui il sulforafano (CH 3 S (O) (CH 2) 4 NCS) dai broccoli, che ha riferito di inibire la crescita tumorale e zwiebelane dagli estratti di cipolla. Il DMSO si trova ampiamente a livelli di tre parti per milione (ppm) o meno ed è un componente comune delle acque naturali, compresa l'acqua di mare. Insieme al dimetil solfone, il DMSO può essere prodotto attraverso il metabolismo delle alghe. Se presente nell'acqua piovana, il DMSO può derivare dall'ossidazione del dimetilsolfuro atmosferico, (CH 3) 2 S, che si verifica come parte del trasferimento naturale di zolfo di origine biologica nel ciclo globale dello zolfo.
I solfossidi sono facilmente preparati mediante ossidazione dei solfuri con reagenti quali metaperiodato di sodio (NaIO 4) o perossido di idrogeno (H 2 O 2). Dal punto di vista commerciale, il DMSO è prodotto dall'ossidazione catalizzata da aria / ossido nitrico di dimetil solfuro, che a sua volta è un sottoprodotto importante del processo di solfato di Kraft per la fabbricazione di carta. Ossidazione più vigorosa di solfuri o solfossidi - come, ad esempio, con permanganato di potassio, KMnO 4 - produce solfoni. I solfossidi otticamente attivi possono essere preparati ossidando i solfuri di tipo RSR ′, dove R ≠ R ′, con ossidanti otticamente attivi o ossidanti microbiologici. In alternativa, i solfossidi otticamente attivi possono essere preparati mediante reazione di derivati sulfinilici otticamente attivi RS (= O) X, dove X = O, N o S, con reagenti come R′Li o R′MgBr. Il solvente solfolano (tiolano S, biossido di S) viene preparato reagendo per primo anidride solforosa con butadiene per dare solfolene (un solfone anulare ciclico, insaturo a cinque membri), seguito da idrogenazione per produrre solfolano.

I solfoni aromatici possono anche essere prodotti dalla reazione di solfonil cloruri con idrocarburi aromatici. Gli ossidi di S e gli S-diossidi di tiofene, formati dall'ossidazione dei tiofeni, sono molto più reattivi dei tiofeni genitore a causa della perdita di aromaticità derivante dalla sostituzione di una o entrambe le coppie di elettroni sullo zolfo con l'ossigeno.













