Aggiunta di nucleofili di carbonio
Un'ampia varietà di nucleofili di carbonio si aggiunge alle aldeidi e tali reazioni sono di primaria importanza nella chimica organica sintetica perché il prodotto è una combinazione di due scheletri di carbonio. I chimici organici sono stati in grado di assemblare quasi qualsiasi scheletro di carbonio, non importa quanto complicato, con usi ingegnosi di queste reazioni. Uno dei più antichi e importanti è l'aggiunta di reagenti Grignard (RMgX, dove X è un atomo alogeno). Il chimico francese Victor Grignard ha vinto il premio Nobel per la chimica del 1912 per la scoperta di questi reagenti e delle loro reazioni.
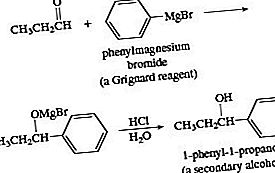
L'aggiunta di un reagente Grignard a un'aldeide seguita dall'acidificazione in acido acquoso dà un alcool. L'aggiunta alla formaldeide dà un alcool primario. L'aggiunta a un'aldeide diversa dalla formaldeide dà un alcool secondario.
Un altro nucleofilo di carbonio è lo ione cianuro, CN -, che reagisce con aldeidi per dare, dopo acidificazione, cianoidrine, composti contenenti un gruppo OH e CN sullo stesso atomo di carbonio.
La benzaldeide cianoidrina (mandelonitrile) fornisce un interessante esempio di meccanismo di difesa chimica nel mondo biologico. Questa sostanza è sintetizzata dai millepiedi (Apheloria corrugata) e immagazzinata in ghiandole speciali. Quando un millepiedi viene minacciato, la cianoidrina viene secreta dalla sua ghiandola di stoccaggio e subisce una dissociazione catalizzata da enzimi per produrre acido cianidrico (HCN). Il millepiedi rilascia quindi il gas HCN nel suo ambiente circostante per scacciare i predatori. La quantità di HCN emessa da un singolo millepiedi è sufficiente per uccidere un piccolo topo. Il mandelonitrile si trova anche nelle mandorle amare e nelle fosse di pesca. La sua funzione è sconosciuta.
Altre reazioni importanti in questa categoria includono la reazione di Knoevenagel, in cui il nucleofilo di carbonio è un estere con almeno un α-idrogeno. In presenza di una base forte, l'estere perde un α-idrogeno per dare un carbonio caricato negativamente che poi si aggiunge al carbonio carbonilico di una aldeide. L'acidificazione seguita dalla perdita di una molecola d'acqua dà un estere α, β-insaturo.
Un'altra reazione di addizione che coinvolge un nucleofilo di carbonio è la reazione di Wittig, in cui una aldeide reagisce con un fosforano (chiamato anche un fosforo ylide), per dare un composto contenente un doppio legame carbonio-carbonio. Il risultato di una reazione di Wittig è la sostituzione dell'ossigeno carbonilico di una aldeide con il gruppo carbonioso legato al fosforo. Il chimico tedesco Georg Wittig ha condiviso il premio Nobel del 1979 in chimica per la scoperta di questa reazione e lo sviluppo del suo uso nella chimica organica sintetica.
I composti contenenti un gruppo trimetilsilile (iSiMe 3, dove Me è il gruppo metile, ―CH 3) e un atomo di litio (Li) sullo stesso atomo di carbonio reagiscono con le aldeidi nella cosiddetta reazione di Peterson per fornire gli stessi prodotti che avrebbero essere ottenuto mediante una corrispondente reazione di Wittig.
Spostamento all'α-carbonio
α-Alogenazione
Un α-idrogeno di una aldeide può essere sostituito da un atomo di cloro (Cl), bromo (Br) o iodio (I) quando il composto viene trattato con Cl 2, Br 2 o I 2, rispettivamente, senza catalizzatore o in presenza di un catalizzatore acido.
La reazione può essere facilmente fermata dopo l'aggiunta di un solo atomo alogeno. L'α-alogenazione si svolge effettivamente sulla forma di enolo (vedi sopra Proprietà delle aldeidi: tautomerismo) dell'aldeide piuttosto che sulla stessa aldeide. La stessa reazione si verifica se viene aggiunta una base, ma non può essere fermata fino a quando tutti gli alogeni α attaccati allo stesso carbonio non saranno sostituiti da atomi di alogeno. Se ci sono tre a-idrogeni sullo stesso atomo di carbonio, la reazione va oltre, causando la scissione di un X 3 C - ion (dove X è un alogeno) e la formazione del sale di un acido carbossilico.

Questa reazione è chiamata reazione dell'aloformio, perché X 3 C - ioni reagiscono con acqua o un altro acido presente nel sistema a composti producono della forma X 3 CH, che sono chiamati aloformi (ad esempio, CHCl 3 si chiama cloroformio).