Francium (Fr), l'elemento chimico più pesante del gruppo 1 (Ia) nella tavola periodica, il gruppo di metalli alcalini. Esiste solo in forme radioattive di breve durata. Il francio naturale non può essere isolato in quantità visibili e pesabili, poiché solo 24,5 grammi (0,86 once) si verificano in qualsiasi momento nell'intera crosta terrestre. L'esistenza del francio è stata predetta dal chimico russo Dmitry I. Mendeleyev nella sua periodica classificazione degli elementi. Il chimico francese Marguerite Perey scoprì il francio (1939) mentre studiava l'attinio-227, che decade per decadimento beta negativo (emissione di elettroni) in un isotopo di torio (torio-227) e per emissione di alfa (circa l'1%) in un isotopo di francio (francio-223) che era precedentemente chiamato attinio K (AcK) ed è un membro della serie di decadimento dell'attinio. Sebbene sia l'isotopo più longevo del francio, il francio-223 ha un'emivita di soli 22 minuti. Trentaquattro isotopi di francio con masse comprese tra 199 e 232 sono stati preparati artificialmente e, poiché il francio naturale non può essere concentrato, viene anche preparato mediante irradiazione di neutroni di radio per produrre attinio, che decade per produrre tracce di francio. La chimica del francio può essere studiata solo con metodi progettati per tracce. Sotto tutti gli aspetti, il suo comportamento osservato, incluso lo stato di ossidazione di +1, è quello che ci si aspetta da un elemento alcalino che riempie un posto appena sotto il cesio nella tavola periodica degli elementi. Non ci sono quasi informazioni sui suoi aspetti biologici.
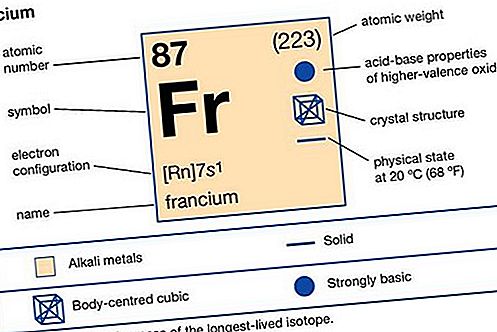

metallo alcalino
cesio (Cs) e francio (Fr). I metalli alcalini sono così chiamati perché la reazione con l'acqua forma alcali (cioè basi forti capaci di
.Proprietà elemento
| numero atomico | 87 |
|---|---|
| isotopo più stabile | (223) |
| stato di ossidazione | +1 |
| configurazione elettronica. | 2-8-18-32-18-8-1 o [Rn] 7s 1 |













