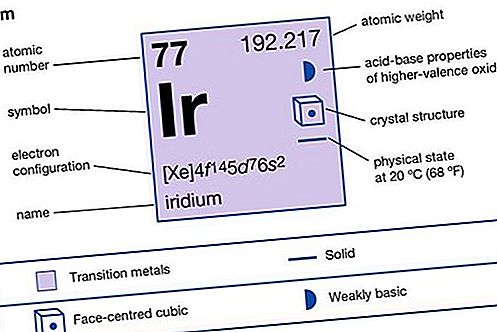
Iridio (Ir), elemento chimico, uno dei metalli del platino dei gruppi 8–10 (VIIIb), periodi 5 e 6, della tavola periodica. È molto denso e raro ed è utilizzato nelle leghe di platino. Un prezioso metallo bianco-argento, l'iridio è duro e fragile, ma diventa duttile e può essere lavorato a un calore bianco, da 1.200 ° a 1.500 ° C (da 2.200 ° a 2.700 ° F). È una delle sostanze terrestri più dense. Allo stato massiccio il metallo è praticamente insolubile in acidi e non viene attaccato nemmeno dall'acqua regia. Può essere sciolto in acido cloridrico concentrato in presenza di perclorato di sodio a 125 ° a 150 ° C (da 257 ° a 302 ° F).
A causa delle difficoltà nella preparazione e nella fabbricazione, il metallo puro ha poche applicazioni. L'iridio è principalmente usato sotto forma di leghe di platino. Le leghe di platino-iridio (dal 5 al 10 percento di iridio) sono metalli facilmente lavorabili che sono molto più duri e rigidi e più resistenti agli attacchi chimici rispetto al morbido platino puro. Tali leghe vengono utilizzate per gioielli, punte di penna, perni e perni chirurgici, contatti elettrici e punti di accensione. Il chilogrammo standard internazionale di massa del prototipo è costituito da una lega contenente il 90% di platino e il 10% di iridio.
L'iridio puro probabilmente non si presenta in natura; la sua abbondanza nella crosta terrestre è molto bassa, circa 0,001 parti per milione. Sebbene raro, l'iridio si presenta nelle leghe naturali con altri metalli nobili: nell'iridosmina fino al 77% di iridio, nel platiniridio fino al 77%, nell'aurosmiridio 52% e nel platino nativo fino al 7,5%. L'iridio viene generalmente prodotto commercialmente insieme agli altri metalli al platino come sottoprodotto della produzione di nichel o rame.
I minerali contenenti iridio si trovano in Sudafrica e in Alaska, negli Stati Uniti, nonché in Myanmar (Birmania), Brasile, Russia e Australia. Alla fine del XX secolo il Sudafrica era il principale produttore mondiale di iridio.
L'elemento fu scoperto nel 1803 nei residui insolubili in acidi dei minerali di platino dal chimico inglese Smithson Tennant; i chimici francesi H.-V. Collet-Descotils, A.-F. Fourcroy e N.-L. Vauquelin lo identificò all'incirca nello stesso momento. Il nome iridio, derivato dalla parola greca iris ("arcobaleno"), si riferisce ai vari colori dei suoi composti. L'iridio naturale è costituito da una miscela di due isotopi stabili, l'iridio-191 (37,3 per cento) e l'iridio-193 (62,7 per cento). La chimica dell'iridio si concentra sugli stati di ossidazione di +1, +3 e +4, sebbene i composti di tutti gli stati da 0 a +6 siano noti con forse l'eccezione di +2. I complessi nello stato di ossidazione +1 contengono principalmente monossido di carbonio, olefine e fosfine come ligandi. Gli anioni esacloroiridato, [IrCl 6] 2−, e esabromoiridato, [IrBr 6] 2−, sono le uniche specie chimiche notevoli contenenti iridio nello stato di ossidazione +4. L'iridio è in qualche modo più reattivo del rutenio e dell'osmio.
Proprietà elemento
| numero atomico | 77 |
|---|---|
| peso atomico | 192,2 |
| punto di fusione | 2.410 ° C (4.370 ° F) |
| punto di ebollizione | 4.527 ° C (8.181 ° F) |
| peso specifico | 22,4 (20 ° C) |
| stati di ossidazione | +1, +3, +4 |
| configurazione elettronica. | [Xe] 4f 14 5d 9 |