Fosforo (P), elemento chimico non metallico della famiglia dell'azoto (Gruppo 15 [Va] della tavola periodica) che a temperatura ambiente è un solido incolore, semitrasparente, morbido, ceroso che si illumina al buio.
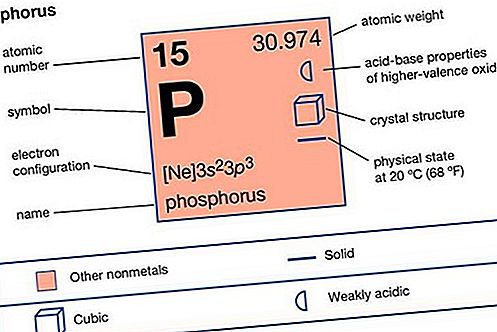
Proprietà elemento
| numero atomico | 15 |
|---|---|
| peso atomico | 30,9738 |
| punto di fusione (bianco) | 44,1 ° C (111,4 ° F) |
| punto di ebollizione (bianco) | 280 ° C (536 ° F) |
| densità (bianco) | 1,82 grammi / cm 3 a 20 ° C (68 ° F) |
| stati di ossidazione | −3, +3, +5 |
| configurazione elettronica | 1s 2 2s 2 2p 6 3s 2 3p 3 |
Storia

Gli alchimisti arabi del XII secolo potrebbero aver isolato il fosforo elementare per caso, ma i dati non sono chiari. Il fosforo sembra essere stato scoperto nel 1669 da Hennig Brand, un commerciante tedesco il cui hobby era l'alchimia. La marca ha permesso a 50 secchi di urina di rimanere in piedi fino a quando non hanno putrefatto e "allevato vermi". Quindi bollì l'urina fino a renderla una pasta e la riscaldò con la sabbia, distillando così il fosforo elementare dalla miscela. Brand riferì la sua scoperta in una lettera a Gottfried Wilhelm Leibniz e, in seguito, dimostrazioni di questo elemento e della sua capacità di brillare nel buio, o "fosforosi", suscitò l'interesse del pubblico. Il fosforo, tuttavia, rimase una curiosità chimica fino a circa un secolo dopo, quando si dimostrò un componente delle ossa. La digestione di ossa con acido nitrico o solforico formava acido fosforico, da cui il fosforo poteva essere distillato riscaldando con carbone. Alla fine del 1800 James Burgess Readman di Edimburgo sviluppò un metodo a fornace elettrica per produrre l'elemento dalla roccia fosfatica, che è essenzialmente il metodo impiegato oggi.
Presenza e distribuzione
Il fosforo è un elemento molto diffuso, il 12 ° più abbondante nella crosta terrestre, al quale contribuisce per circa lo 0,10 percento in peso. La sua abbondanza cosmica è di circa un atomo per 100 atomi di silicio, lo standard. La sua elevata reattività chimica assicura che non si verifichi allo stato libero (tranne in alcuni meteoriti). Il fosforo si presenta sempre come ione fosfato. Le principali forme combinate in natura sono i sali di fosfato. È stato scoperto che circa 550 minerali diversi contengono fosforo, ma, di questi, la principale fonte di fosforo è la serie di apatite in cui esistono ioni calcio con ioni fosfato e quantità variabili di ioni fluoruro, cloruro o idrossido, secondo la formula [Ca 10 (PO 4) 6 (F, Cl o OH) 2]. Altri importanti minerali contenenti fosforo sono la wavellite e la vivianite. Comunemente, atomi di metallo come magnesio, manganese, stronzio e piombo sostituiscono il calcio nel minerale e silicati, solfati, vanadati e analoghi sostituti sostituiscono gli ioni fosfato. Depositi sedimentari molto grandi di fluoroapatite si trovano in molte parti della Terra. Il fosfato di smalto osseo e dentale è idrossiapatite. (Il principio di riduzione della carie dentale mediante fluoridazione dipende dalla conversione dell'idrossiapatite in fluoroapatite più dura, più resistente alla decomposizione.)
La principale fonte commerciale è la fosforite, o roccia fosfatica, una forma impura e massiccia di apatite contenente carbonato. Le stime della roccia totale di fosfato nella crosta terrestre sono in media di circa 65.000.000.000 di tonnellate, di cui il Marocco e il Sahara occidentale contengono circa l'80%. Questa stima include solo minerale sufficientemente ricco di fosfato per la conversione in prodotti utili con i metodi attuali. Esistono anche grandi quantità di materiale a basso contenuto di fosforo.

L'unico isotopo naturale del fosforo è quello della massa 31. Gli altri isotopi dalla massa 24 alla massa 46 sono stati sintetizzati da appropriate reazioni nucleari. Tutti questi sono radioattivi con emivite relativamente brevi. L'isotopo di massa 32 ha un'emivita di 14.268 giorni e si è dimostrato estremamente utile negli studi sui traccianti che coinvolgono l'assorbimento e il movimento del fosforo negli organismi viventi.