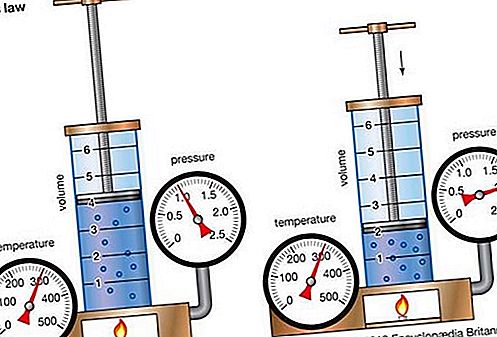
La legge di Boyle, chiamata anche legge di Mariotte, una relazione riguardante la compressione e l'espansione di un gas a temperatura costante. Questa relazione empirica, formulata dal fisico Robert Boyle nel 1662, afferma che la pressione (p) di una data quantità di gas varia inversamente con il suo volume (v) a temperatura costante; cioè, in forma di equazione, pv = k, una costante. La relazione fu scoperta anche dal fisico francese Edme Mariotte (1676).
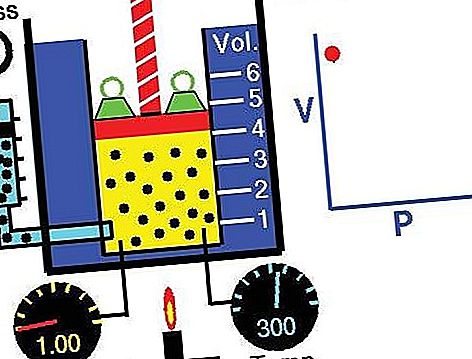
La legge può essere derivata dalla teoria cinetica dei gas ipotizzando un gas perfetto (ideale) (vedi gas perfetto). I gas reali obbediscono alla legge di Boyle a pressioni sufficientemente basse, sebbene il pv del prodotto generalmente diminuisca leggermente a pressioni più elevate, dove il gas inizia a discostarsi dal comportamento ideale.