Proprietà elastiche
Come con la maggior parte delle altre proprietà dei metalli delle terre rare, i moduli elastici dei metalli delle terre rare cadono nel percentile medio degli altri elementi metallici. I valori di scandio e ittrio sono all'incirca gli stessi dei membri finali dei lantanidi (da erbio a lutetio). C'è un aumento generale del modulo elastico con l'aumentare del numero atomico. Sono evidenti i valori anomali per cerio (alcuni legami 4f) e itterbio (divalenza).
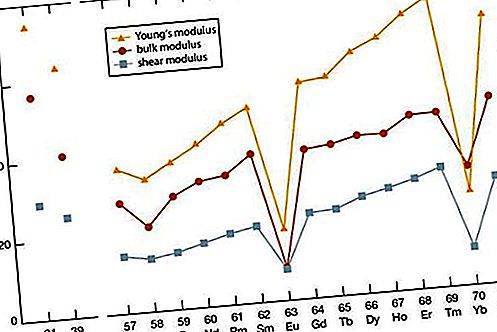
Proprietà meccaniche
I metalli delle terre rare non sono né elementi metallici deboli né particolarmente forti e presentano una duttilità modesta. Poiché le proprietà meccaniche dipendono fortemente dalla purezza dei metalli e dalla loro storia termica, è difficile confrontare i valori riportati in letteratura. La forza finale varia da circa 120 a circa 160 MPa (megapascal) e la duttilità da circa il 15 a 35 percento. La forza di itterbio (europio non è stata misurata) è molto più piccola, 58 MPa, e la duttilità è maggiore, circa il 45 percento, come ci si aspetterebbe dal metallo bivalente.
Proprietà chimiche
La reattività dei metalli delle terre rare con l'aria presenta una differenza significativa tra i lantanidi leggeri e quelli pesanti. I lantanidi leggeri si ossidano molto più rapidamente rispetto ai lantanidi pesanti (gadolinio attraverso il lutezio), lo scandio e l'ittrio. Questa differenza è in parte dovuta alla variazione del prodotto ossido formato. I lantanidi leggeri (da lantanio a neodimio) formano la struttura esagonale di tipo A R 2 O 3; i lantanidi medi (samario attraverso gadolinio) formano la fase monoclina di tipo B R 2 O 3; mentre i lantanidi pesanti, lo scandio e l'ittrio formano la modifica cubica di tipo C R 2 O 3. Il tipo A reagisce con il vapore acqueo nell'aria formando un ossidrossido, che provoca lo spallamento del rivestimento bianco e consente all'ossidazione di procedere esponendo la superficie metallica fresca. L'ossido di tipo C forma un rivestimento stretto e coerente che impedisce l'ulteriore ossidazione, simile al comportamento dell'alluminio. Il samario e il gadolinio, che formano la fase R 2 O 3 di tipo B, si ossidano leggermente più velocemente rispetto ai lantanidi, allo scandio e all'ittrio più pesanti, ma formano ancora un rivestimento coerente che blocca l'ulteriore ossidazione. Per questo motivo, i lantanidi leggeri devono essere conservati sotto vuoto o in atmosfera di gas inerte, mentre i lantanidi pesanti, lo scandio e l'ittrio possono essere lasciati all'aperto per anni senza ossidazione.
Il metallo Europium, che ha una struttura ccn, ossida il più rapidamente tra le terre rare con aria umida e deve essere maneggiato in ogni momento in atmosfera di gas inerte. Il prodotto di reazione dell'Europio quando esposto all'aria umida è un idrossido idrato, Eu (OH) 2 ―H 2 O, che è un prodotto di reazione insolito perché tutti gli altri metalli delle terre rare formano un ossido.
I metalli reagiscono vigorosamente con tutti gli acidi tranne l'acido fluoridrico (HF), rilasciando gas H 2 e formando il corrispondente composto anione-terre rare. I metalli delle terre rare se posti in acido fluoridrico formano un rivestimento insolubile RF 3 che impedisce qualsiasi ulteriore reazione.
I metalli delle terre rare reagiscono prontamente con idrogeno gassoso formando RH 2 e, in condizioni di forte idratazione, la fase RH 3, tranne lo scandio, che non forma un triidruro.
Composti
Gli elementi delle terre rare formano decine di migliaia di composti con tutti gli elementi a destra del - incluso il gruppo 7 metalli (manganese, tecnezio e renio) nella tavola periodica, più il berillio e il magnesio, che giacciono in lontananza lato sinistro nel gruppo 2. Di seguito sono descritte importanti serie di composti e alcuni singoli composti con proprietà uniche o comportamenti insoliti.
ossidi
La più grande famiglia di composti inorganici di terre rare studiata fino ad oggi sono gli ossidi. La stechiometria più comune è la composizione di R 2 O 3, ma, poiché alcuni elementi di lantanide hanno altri stati di valenza oltre a 3+, esistono altre stechiometrie, ad esempio ossido di cerio (CeO 2), ossido di praseodimio (Pr 6 O 11), ossido di terbio (Tb 4 O 7), ossido di europio (EuO) ed Eu 3 O 4. La maggior parte della discussione verterà sugli ossidi binari, ma anche brevemente verranno esaminati brevemente ternari e altri ossidi di ordine superiore.












![Film animato di Biancaneve e i sette nani [1937] Film animato di Biancaneve e i sette nani [1937]](https://images.thetopknowledge.com/img/entertainment-pop-culture/6/snow-white-seven-dwarfs-animated-film-1937.jpg)